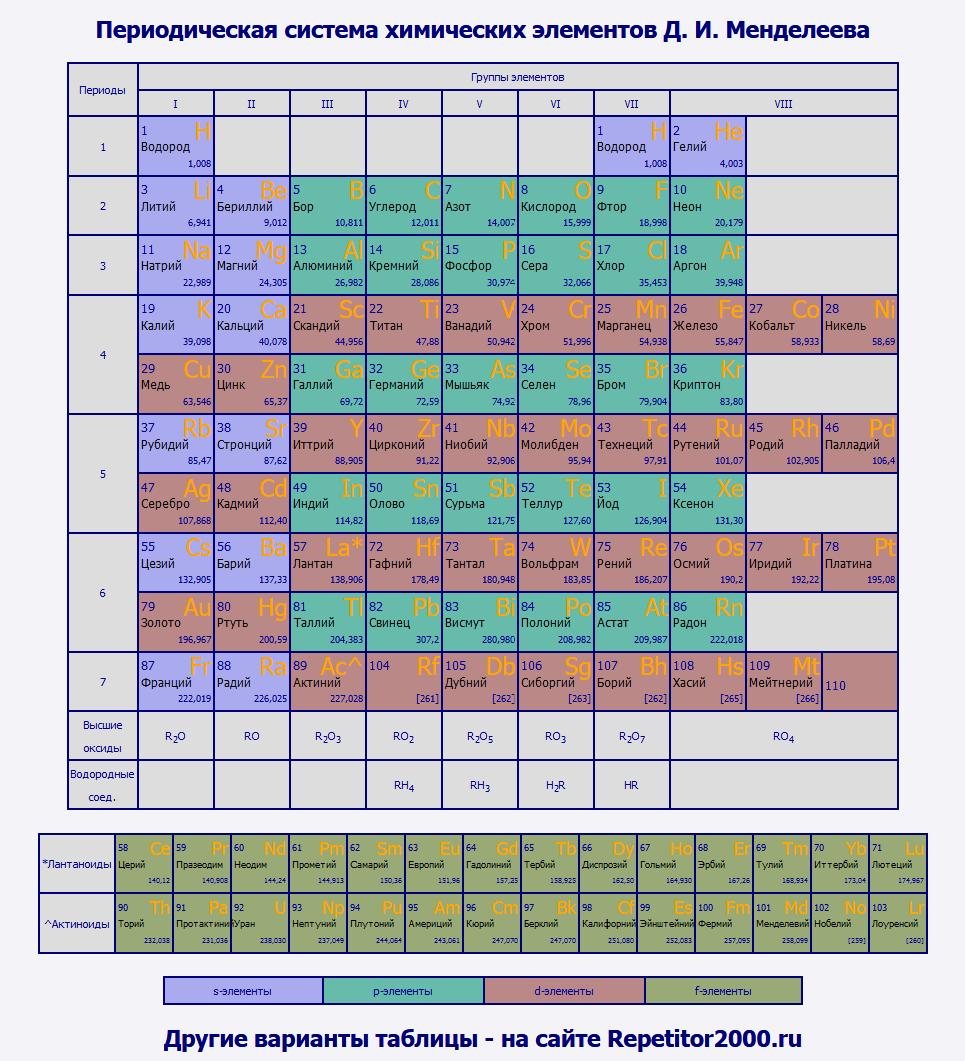
Почему хлор и марганец расположены в одной группе но в разных подгруппах
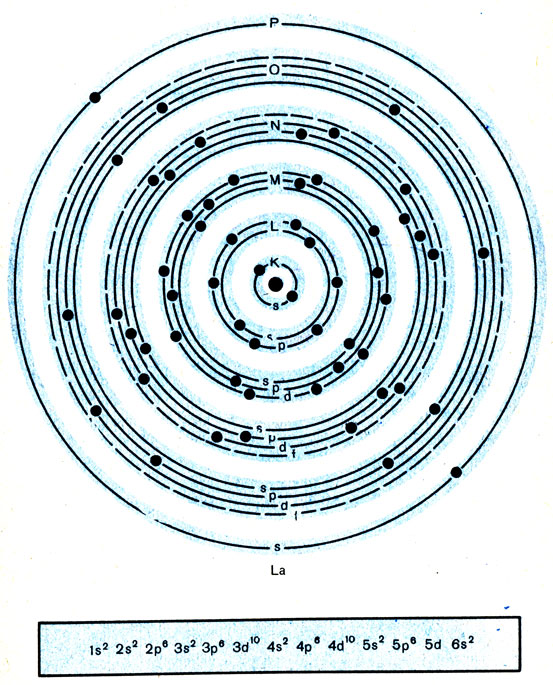
Особенности строения электронных оболочек атомов элементов
Phone or email. Задача 40 Определить частоту света, излучаемого при переходе электрона в атоме водорода с третьего энергетического уровня на второй. Задача 42 На каком основании хлор и марганец помещают в одной группе периодической системы элементов? Почему их помещают в разных подгруппах?
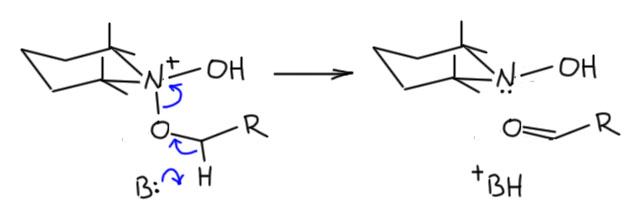



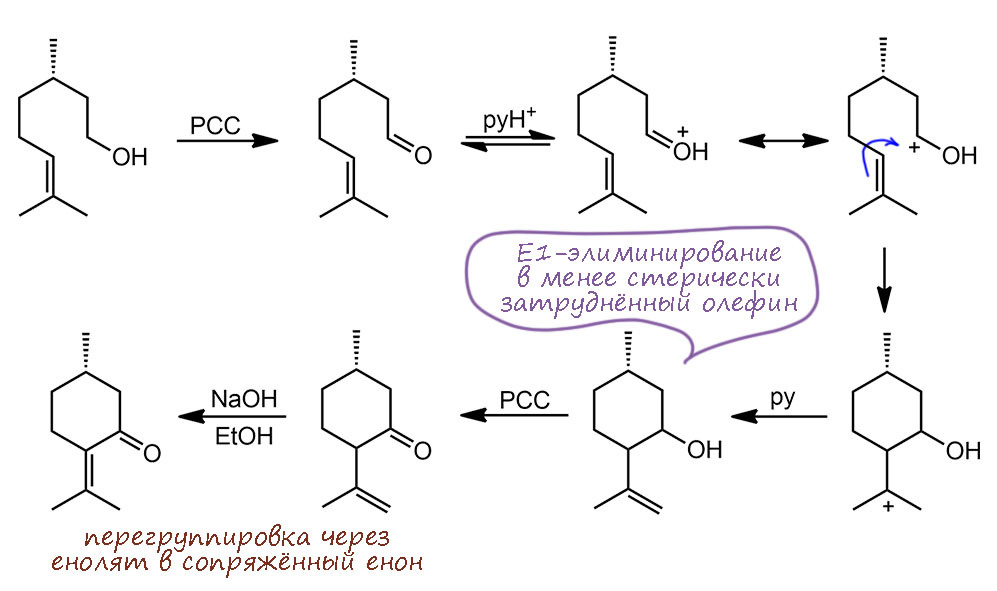
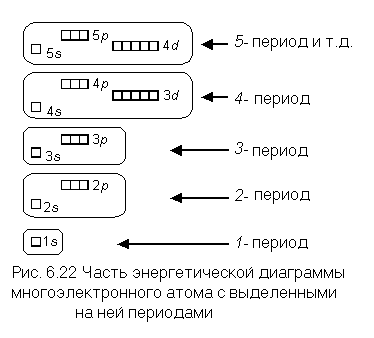
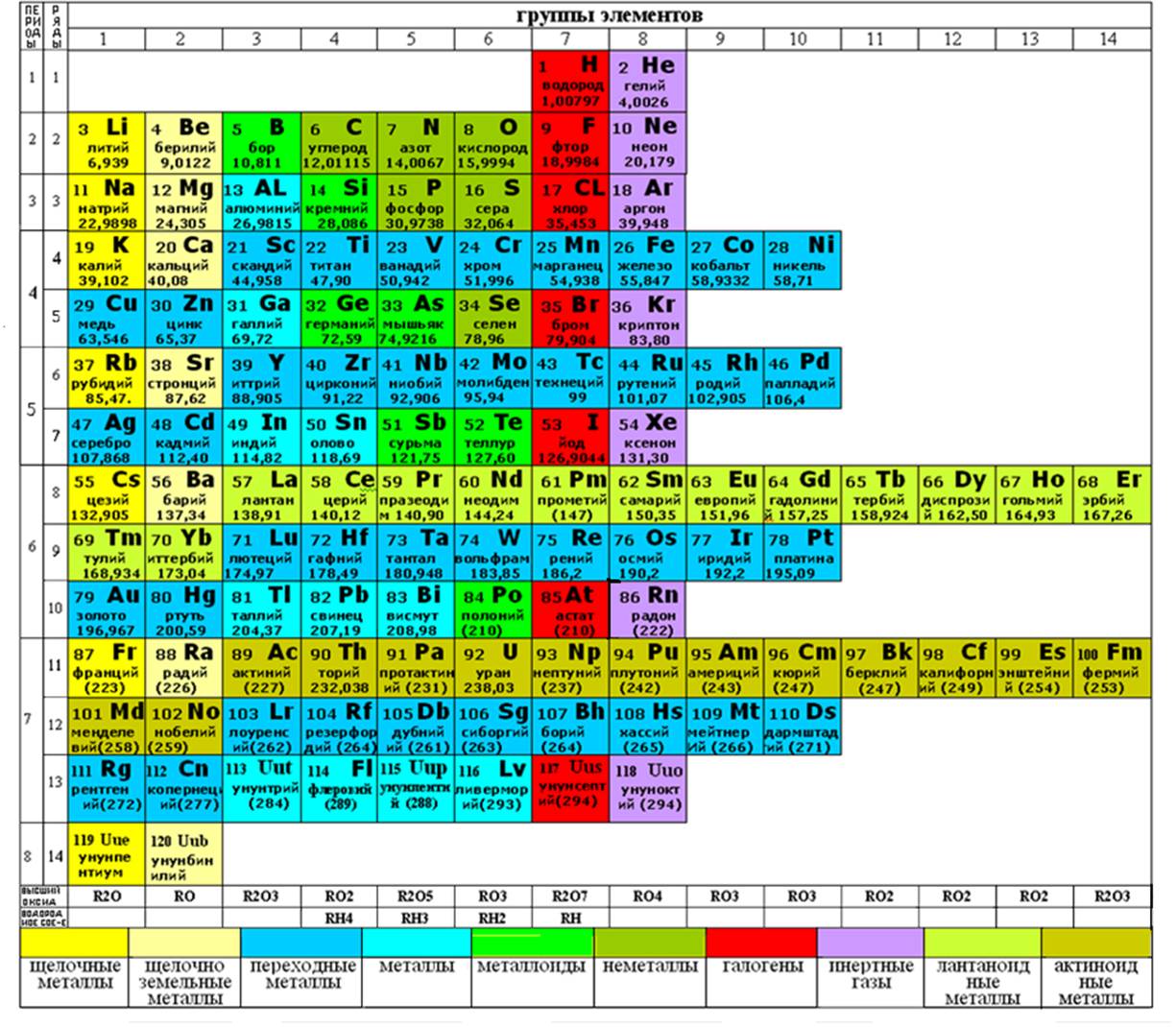
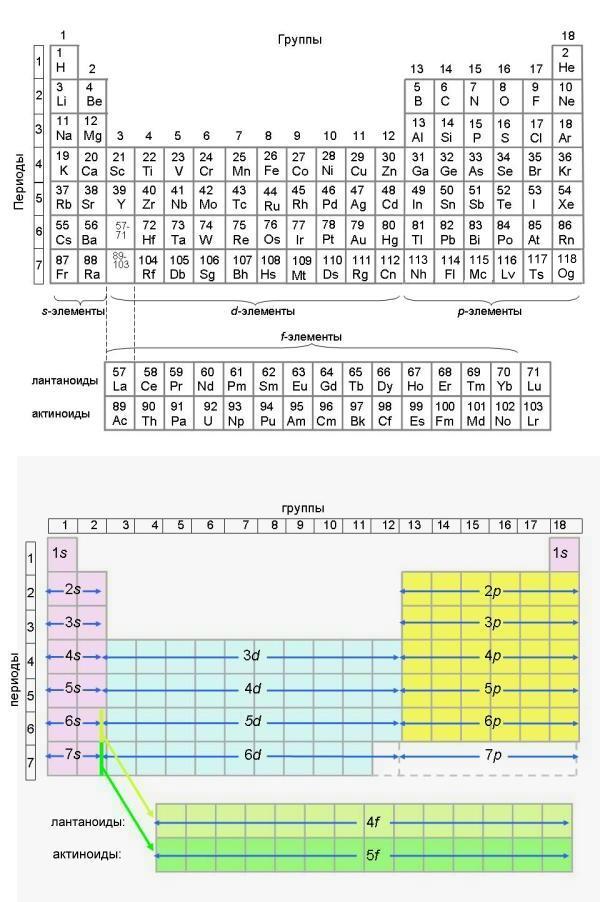


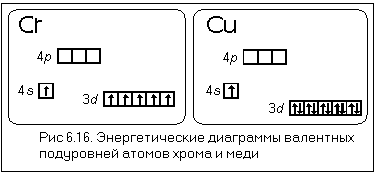
Если вы внимательно посмотрели приложение 4, то, наверное, заметили, что у атомов некоторых элементов последовательность заполнения электронами орбиталей нарушается. Иногда эти нарушения называют "исключениями ", но это не так — исключений из законов Природы не бывает! Первым элементом с таким нарушением является хром.
- Сейчас в обществе все больше набирает оборот модный тренд — минималистичный образ жизни. Как в фильме «Сто вещей и ничего лишнего».
- Составьте электронные формулы атомов марганца и хлора. Отметьте, в чём сходство и различие в строении атомов этих химических элементов.
- НГТУ им.
- Описание поведения даже только двух электронов в атоме оказывается непосильной задачей для современной вычислительной науки, поэтому предполагается, что любой многоэлектронный атом похож энергетические уровни, форма орбиталей и другие свойства на атом водорода. Однако для такого предположения приходится вводить целый ряд дополнительных теоретических предпосылок.
- Возбужденное состояние.
- Соединения марганца, железа и хрома встречаются не только во многих задачах в учебнике, но и в повседневной жизни — стоит вспомнить, например, ржавчину на капоте машины или кране в ванной, раствор марганцовки, которым мы обрабатываем раны, или красиво переливающиеся хромированные автомобили.
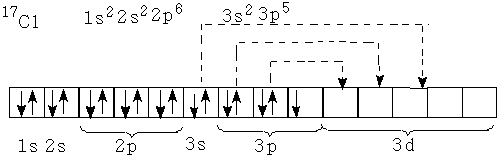

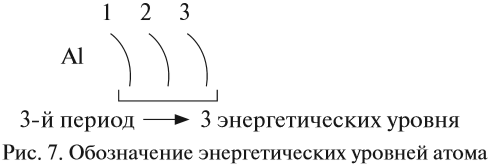
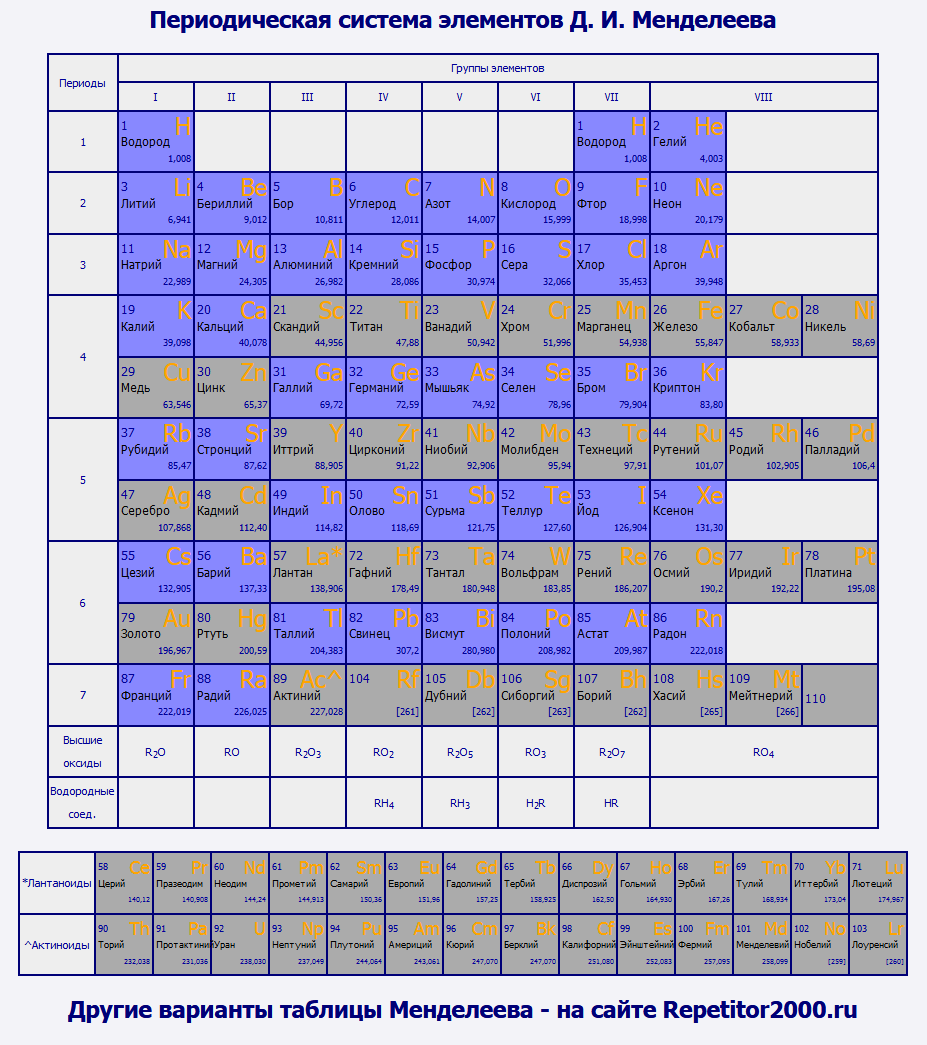
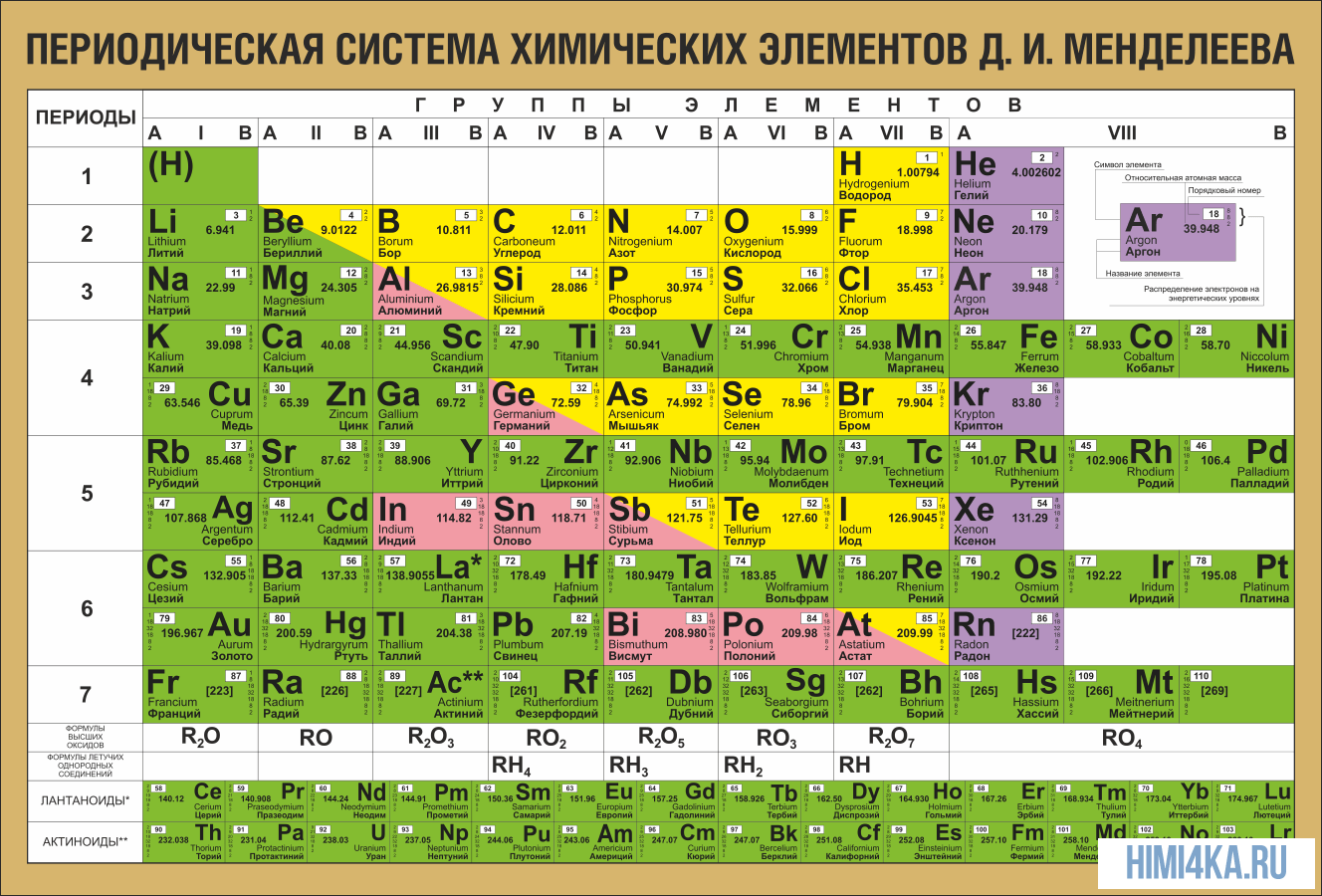



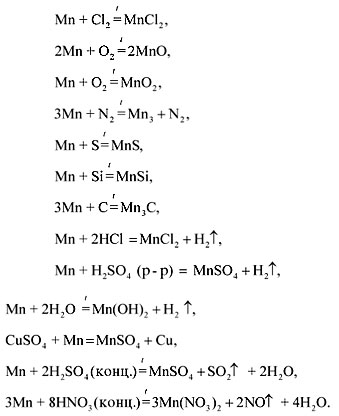
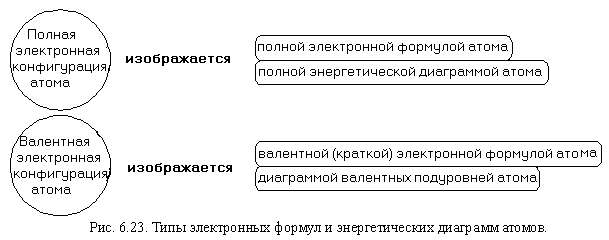
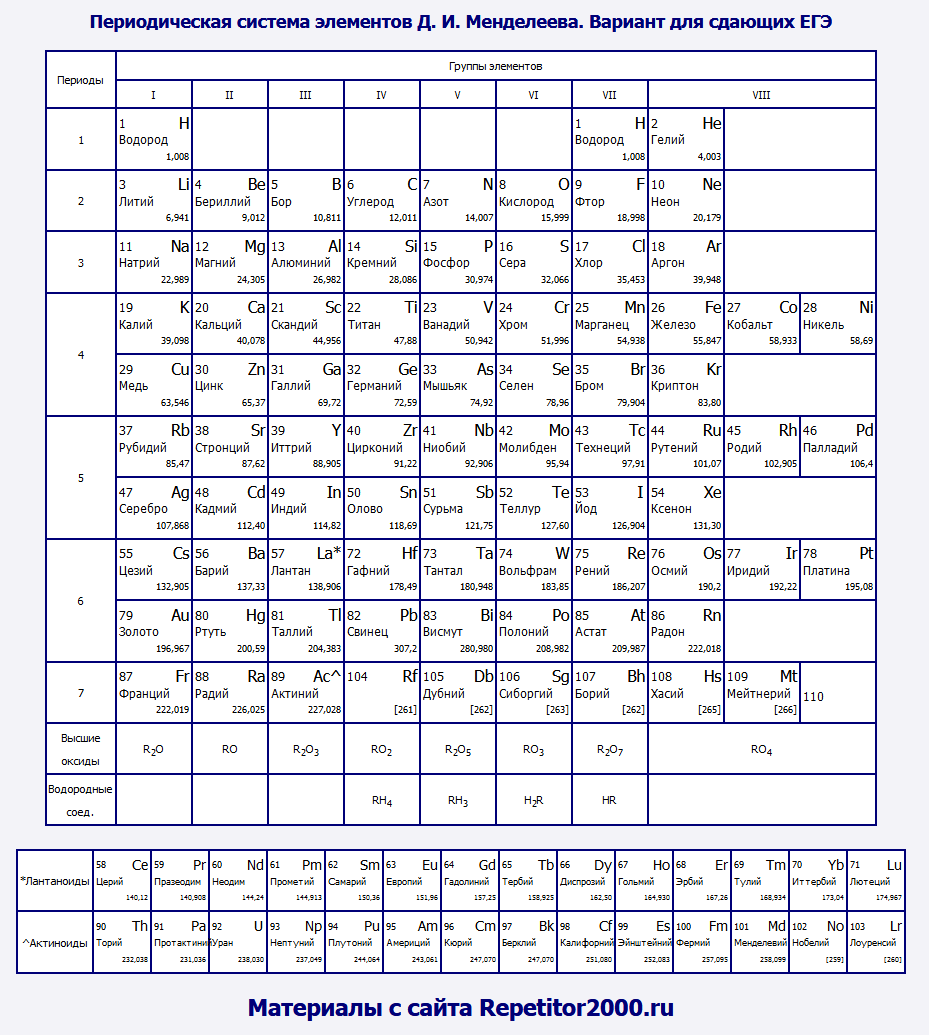
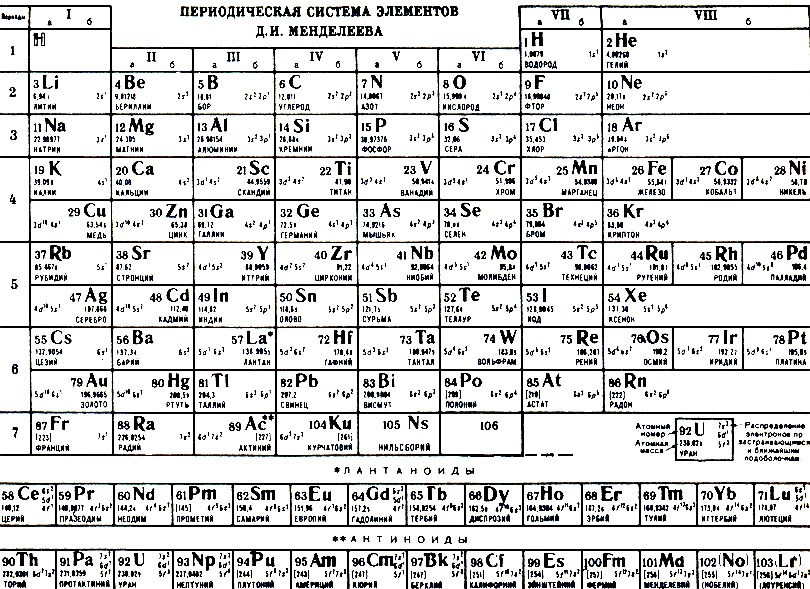
Химические свойства элементов зависят от строения их атомов и положения в периодической системе. При химических реакциях происходит перестройка электронных оболочек атомов — изменение электронной конфигурации внешнего энергетического уровня. Причиной этого является стремление атомов к приобретению наиболее устойчивого состояния, при котором энергетический уровень максимально заполнен электронами. Энергетические уровни и подуровни, полностью заполненные электронами, называются завершенными. Они не вступают в химические реакции за исключением Xe. У атомов всех других химических элементов внешние энергетические уровни незавершенные.